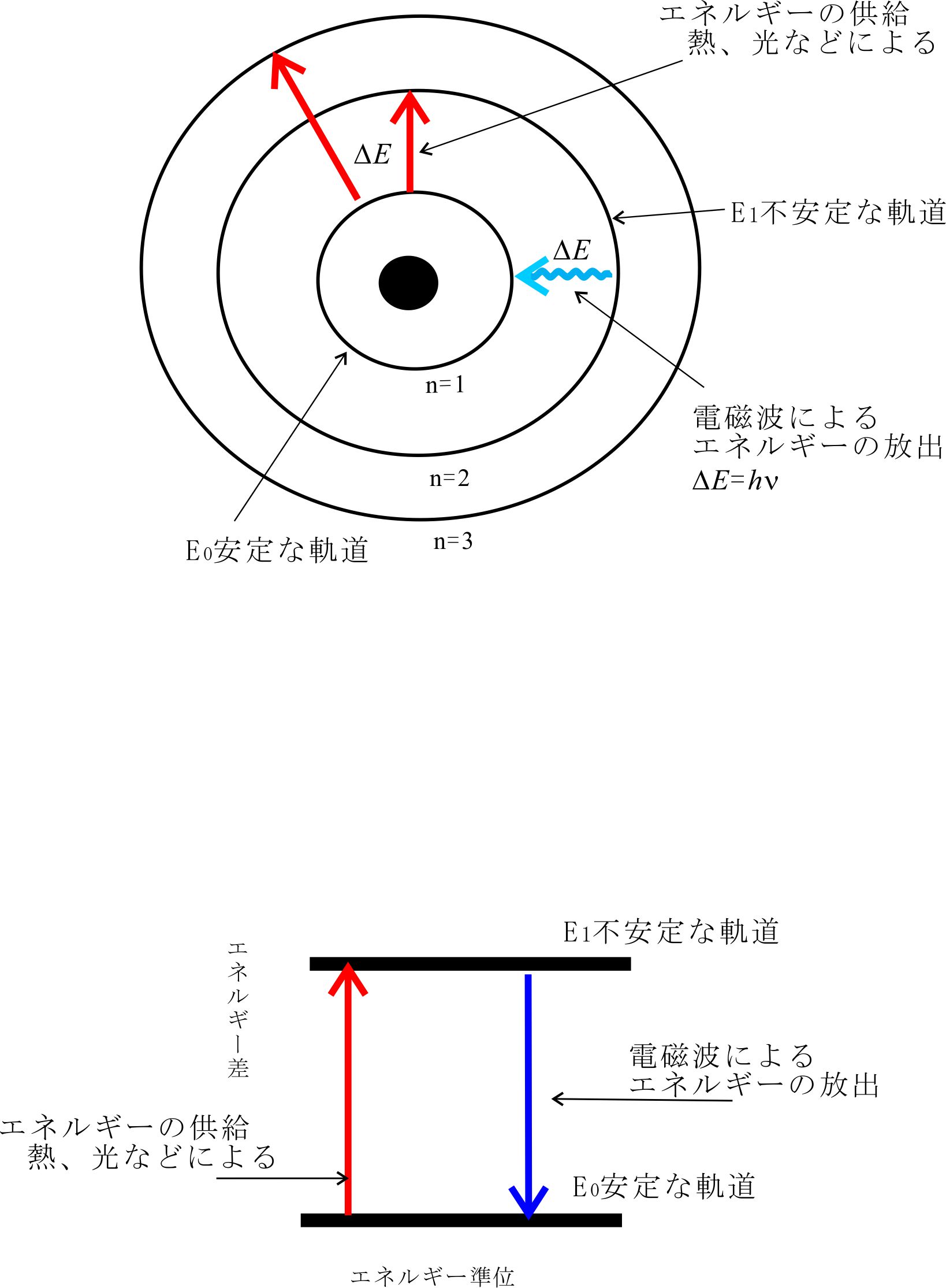
図1 原子の軌道とエネルギー遷移
この励起状態は不安定なので,励起された電子はしばらくしてもとの基底状態[E0]に戻ります。 この電子が低いエネルギー状態に移るときに,二つの状態の差に相当するエネルギーを光として放出します。 この光の波長が可視領域(400nm-700nm)にあるとき,表1に示したような金属固有の色の炎が見えることになります。
燃える
人は火を使うようになってから暖を取り、料理し、暗い闇を照らし、道具を作るために使ってきました。しかしラボアゼが燃えることは酸化で酸素と反応することであることを確定するまで,フロジストン説などが提出され、多くの時間を必要としました。
① 燃えるものなし の実験
② 酸素を断った実験(無酸素実験、窒素やCO2等との置換実験、酸素下での実験との比較)
③ 発火温度より下げた条件での実験
炎色反応


図2 金属の炎色反応 1)
表1 金属と炎色
|
元素名 |
炎 色 |
元素名 |
炎 色 |
|
リチウム |
深赤(紅) |
カルシウム |
黄赤(橙赤) |
|
ナトリウム |
黄色 |
ストロンチウム |
赤 |
|
カリウム |
淡紫 |
バリウム |
淡黄緑 |
|
ルビジウム |
深紅(赤) |
銅 |
濃緑(青緑) |
|
セシウム |
青紫 |
インジウム |
深青 |

図3 黒いほのお
また炎色反応中のナトリウムに低圧ナトリウムランプのD線(589.59 nmおよび589.00
nm)を当てると図3のような黒い炎が見えます。これは燃えている炎色反応の炎の中にはナトリウム原子が存在します。このナトリウム原子がナトリウムのD線の光を吸収するため、光が通らなくその部分が黒く見えています。
この原理は微量の金属の定量測定に使われています。(原子吸光分析)
1) 木村,新居, "演示実験や体験実験のための炎色反応", 近畿大学理工学総合研究所紀要, 30 ,31-36(2018).
Final update 2021.4.2
Copyright (c) 2015 NaniwaKoubou All Rights Reserved.